プレスリリース 発行No.1083 令和2年6月17日
短鎖ヘアピンDNAによる高感度生体分子検出法の開発
~ 1分子イメージング可能な染色法 ~
~ 1分子イメージング可能な染色法 ~
東邦大学医学部解剖学講座の恒岡洋右講師と船戸弘正教授は、新しく開発した短い配列のDNAを用いて高感度な生体分子を検出する方法(in situ hybridization chain reaction法、以下in situ HCR法)を開発しました。
これは既存のin situ HCR法で用いられてきたDNAの配列を改良し、大幅なコスト減が可能となるものです。
これにより、今後組織学におけるイメージング技術の発展はもとより、臨床現場における病原体の検出などにも応用されることが期待されます。
この成果は2020年5月12日に雑誌Frontiers in Molecular Neuroscience誌にて発表され、2020年6月12日に特許出願されました。
これは既存のin situ HCR法で用いられてきたDNAの配列を改良し、大幅なコスト減が可能となるものです。
これにより、今後組織学におけるイメージング技術の発展はもとより、臨床現場における病原体の検出などにも応用されることが期待されます。
この成果は2020年5月12日に雑誌Frontiers in Molecular Neuroscience誌にて発表され、2020年6月12日に特許出願されました。
発表者名
恒岡 洋右(東邦大学医学部解剖学講座微細形態学分野 講師)
船戸 弘正(東邦大学医学部解剖学講座微細形態学分野 教授)
船戸 弘正(東邦大学医学部解剖学講座微細形態学分野 教授)
発表のポイント
- 短いヘアピン型DNAであっても高効率・低ノイズでhybridization chain reaction 反応を誘導することが出来る配列を発見した。
- DNA鎖長を既存の配列の半分近くまで減らすことで組織への浸透性を上昇させると共に大幅なコストカットが実現可能となった。
発表概要
組織における様々な遺伝子の発現やタンパク質量のモニターは生命現象を理解する上では無くてはなりません。これまでも多くの研究室や臨床現場で様々な生体分子の検出が行われて、その手法は改良され続けてきました。
近年の技術の発展に伴い、高感度・低ノイズを謳った手法が考案されてきましたが、その多くは高価で、普及の壁となっています。
その中で、研究グループは蛍光DNAを用いて生体分子を組織で検出するこれまでのin situ HCR法を改良し、DNA配列を短くして低コスト化するとともに、様々なDNAの標識法を検討することで、高効率・低ノイズでin situ HCR法を実現することを可能としました。この手法では、Proteinase K処理という操作を必要とせず免疫染色(注1)との組み合わせが可能で、複数の標的分子の検出が一種類の分子の検出と同じスピードで出来る簡便さも兼ね備えています。
近年の技術の発展に伴い、高感度・低ノイズを謳った手法が考案されてきましたが、その多くは高価で、普及の壁となっています。
その中で、研究グループは蛍光DNAを用いて生体分子を組織で検出するこれまでのin situ HCR法を改良し、DNA配列を短くして低コスト化するとともに、様々なDNAの標識法を検討することで、高効率・低ノイズでin situ HCR法を実現することを可能としました。この手法では、Proteinase K処理という操作を必要とせず免疫染色(注1)との組み合わせが可能で、複数の標的分子の検出が一種類の分子の検出と同じスピードで出来る簡便さも兼ね備えています。
発表内容
組織における様々な遺伝子の発現やタンパク質量のモニターは生命現象を理解する上では無くてはならないものです。mRNAは核内のDNAの遺伝子情報が転写され細胞内へと情報を運び、タンパク質などの物質合成に関わります。遺伝子ごと・細胞ごとにmRNAの量は多様で、これが細胞の役割を決定付けます。このmRNAを検出する方法は酵素を用いた方法がこれまで主に用いられてきましたが、検出感度が低いことや検出までにかかる時間が長かったり、作業量が多いことが欠点でした。近年、酵素を用いずに人工合成したDNAを用いてmRNAを高感度に検出する手法が複数開発されてきましたが、その多くは非常に高額で、研究者や臨床現場においては普及の壁となってきました。in situ HCR法は蛍光標識されたヘアピン型の合成DNAを用いる手法として知られています。この手法は、組織内でヘアピンDNAを非酵素的に重合させることで1分子のmRNAを検出できる感度を持ち、検出までにかかる時間が短いという利点を持ちますが、検出に用いるヘアピンDNAの鎖長が長く、純度の高いDNAの合成が難しいため高額なものでした。
そこで研究グループは、より安価にmRNAの高感度検出を行うため、このヘアピンDNAの鎖長を短くする試みを行いました。DNAの鎖長を減らすとDNAのヘアピン構造の安定性が低下し非特異的な反応が起こることや、重合反応の効率が落ちることが知られています。この問題を解決するため、用いるヘアピンDNAの安定性に関わるstem部位の配列と重合反応の効率に関わるtoehold部位の配列を検討し、短いヘアピンDNAであっても安定性を維持し重合反応の効率の高いDNA配列を複数見出し、その配列の法則を発見しました(図1)。また、DNAの標識に用いるアミノリンカー(注2)や蛍光色素についても最適な条件を見出すことに成功しました。これらの改良により、DNAの合成にかかる費用は60%以上減少しました。
新たに開発したこの短鎖ヘアピンDNAを用いて実際に組織内でのmRNAの検出を試みたところ、既存の長いヘアピンDNAを用いた場合と同様に1分子のmRNA検出が可能であり(図2)、さらに酵素を用いたmRNA検出よりも高感度であることが示されました。また、同時に複数種類のmRNAを異なる波長の色素で検出することが可能であり、これまで数日から1週間かかっていた検出操作が24時間以内に終わり、既存のin situ HCR法と同様の長所を持つことが明らかになりました。
これらの特徴に加えて、ヘアピンDNAの鎖長を短くしたことによりDNA分子の組織内への浸透性が向上し、細胞膜を破壊するようなProteinase K処理などの手法を用いずともmRNAの検出感度が落ちないという長所も明らかになりました(図3)。これまでmRNAの検出の前処理として広く用いられてきたProteinase K処理は、細胞膜だけでなく細胞内のタンパク質も破壊するために、組織でタンパク質とmRNAを同時に検出しにくいという問題がありました。短鎖ヘアピンDNAを用いたin situ HCR法では、Proteinase K 処理が不要であるためにmRNAとタンパク質を同時に検出することも容易になり、今後様々な研究に応用される基盤技術となることが期待されます。
そこで研究グループは、より安価にmRNAの高感度検出を行うため、このヘアピンDNAの鎖長を短くする試みを行いました。DNAの鎖長を減らすとDNAのヘアピン構造の安定性が低下し非特異的な反応が起こることや、重合反応の効率が落ちることが知られています。この問題を解決するため、用いるヘアピンDNAの安定性に関わるstem部位の配列と重合反応の効率に関わるtoehold部位の配列を検討し、短いヘアピンDNAであっても安定性を維持し重合反応の効率の高いDNA配列を複数見出し、その配列の法則を発見しました(図1)。また、DNAの標識に用いるアミノリンカー(注2)や蛍光色素についても最適な条件を見出すことに成功しました。これらの改良により、DNAの合成にかかる費用は60%以上減少しました。
新たに開発したこの短鎖ヘアピンDNAを用いて実際に組織内でのmRNAの検出を試みたところ、既存の長いヘアピンDNAを用いた場合と同様に1分子のmRNA検出が可能であり(図2)、さらに酵素を用いたmRNA検出よりも高感度であることが示されました。また、同時に複数種類のmRNAを異なる波長の色素で検出することが可能であり、これまで数日から1週間かかっていた検出操作が24時間以内に終わり、既存のin situ HCR法と同様の長所を持つことが明らかになりました。
これらの特徴に加えて、ヘアピンDNAの鎖長を短くしたことによりDNA分子の組織内への浸透性が向上し、細胞膜を破壊するようなProteinase K処理などの手法を用いずともmRNAの検出感度が落ちないという長所も明らかになりました(図3)。これまでmRNAの検出の前処理として広く用いられてきたProteinase K処理は、細胞膜だけでなく細胞内のタンパク質も破壊するために、組織でタンパク質とmRNAを同時に検出しにくいという問題がありました。短鎖ヘアピンDNAを用いたin situ HCR法では、Proteinase K 処理が不要であるためにmRNAとタンパク質を同時に検出することも容易になり、今後様々な研究に応用される基盤技術となることが期待されます。
発表雑誌
-
雑誌名
「Frontiers in Molecular Neuroscience」(2020年5月12日)
論文タイトル
Modified in situ hybridization chain reaction using short hairpin DNAs
著者
Yousuke Tsuneoka* and Hiromasa Funato* (* 責任著者)
DOI番号
doi: 10.3389/fnmol.2020.00075
アブストラクトURL
https://www.frontiersin.org/articles/10.3389/fnmol.2020.00075/abstract
用語解説
(注1)免疫染色
タンパク質を検出するための手法。タンパク質に特異的な抗体によってタンパク質を標識して可視化することができる。
(注2)アミノリンカー
DNAを蛍光色素と結合させるための化学構造。サクシニミジルエステル基を持つ蛍光色素と反応し、アミド結合によってDNAに蛍光色素を標識させることができる。
タンパク質を検出するための手法。タンパク質に特異的な抗体によってタンパク質を標識して可視化することができる。
(注2)アミノリンカー
DNAを蛍光色素と結合させるための化学構造。サクシニミジルエステル基を持つ蛍光色素と反応し、アミド結合によってDNAに蛍光色素を標識させることができる。
添付資料
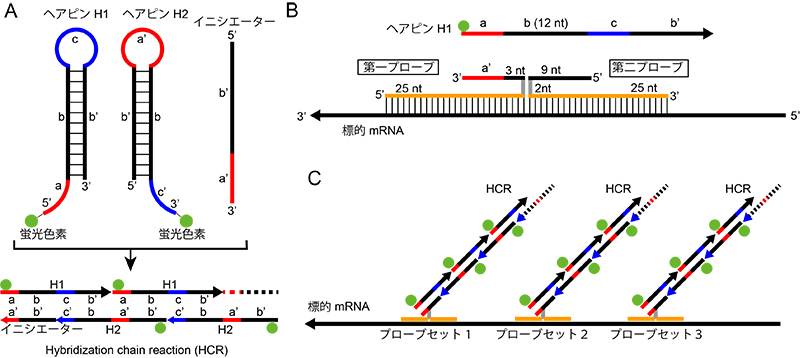
図1.in situ HCR 法の原理と短鎖ヘアピンDNAの設計
A. アルファベットの’は相補配列を示す。鎖置換反応によってイニシエーターa’b’とヘアピンH1が結合すると、H1のcb’配列が露出する。H1のcとb’配列はH2のイニシエーターとなり、H2と結合し、H2はa’b’配列を露出する。a’b’配列はH1と結合する。
このイニシエーターを開始剤として、蛍光標識されたヘアピンDNAが重合していく。
B, C. イニシエーターの末端に標的mRNAと相補な配列を導入したプローブにより、プローブがmRNAと結合することでHCRが開始する。
A. アルファベットの’は相補配列を示す。鎖置換反応によってイニシエーターa’b’とヘアピンH1が結合すると、H1のcb’配列が露出する。H1のcとb’配列はH2のイニシエーターとなり、H2と結合し、H2はa’b’配列を露出する。a’b’配列はH1と結合する。
このイニシエーターを開始剤として、蛍光標識されたヘアピンDNAが重合していく。
B, C. イニシエーターの末端に標的mRNAと相補な配列を導入したプローブにより、プローブがmRNAと結合することでHCRが開始する。

図2. 分界条床核におけるオキシトシンmRNAの検出
Hoechstによって核を青に、in situ HCR法によってオキシトシンmRNAを緑に染色した。
オキシトシンmRNA1分子が1個の緑色の顆粒として可視化されている。
Hoechstによって核を青に、in situ HCR法によってオキシトシンmRNAを緑に染色した。
オキシトシンmRNA1分子が1個の緑色の顆粒として可視化されている。

図3. Proteinase K処理によるmRNAとタンパク質検出への影響
(上段)Proteinase K処理あり(下段)Proteinase K処理なし
Vglut2 mRNA(マゼンタ)の感度はProteinase K処理の影響を受けないが、
c-FosタンパクはProteinase K処理によって検出できなくなる。
(上段)Proteinase K処理あり(下段)Proteinase K処理なし
Vglut2 mRNA(マゼンタ)の感度はProteinase K処理の影響を受けないが、
c-FosタンパクはProteinase K処理によって検出できなくなる。
以上
お問い合わせ先
【本発表資料のお問い合わせ先】
東邦大学医学部解剖学講座微細形態学分野
講師 恒岡 洋右
教授 船戸 弘正
〒143-8540 大田区大森西5-21-16
TEL: 03-3762-4151 FAX: 03-5493-5437
E-mail: yousuke.tsuneoka[@]med.toho-u.ac.jp(恒岡)
E-mail: hiromasa.funato[@]med.toho-u.ac.jp (船戸)
URL:http://toho-funatolab.jp/
【本ニュースリリースの発信元】
学校法人東邦大学 法人本部経営企画部
〒143-8540 大田区大森西5-21-16
TEL: 03-5763-6583 FAX: 03-3768-0660
E-mail: press[@]toho-u.ac.jp
URL:www.toho-u.ac.jp
※E-mailはアドレスの[@]を@に替えてお送り下さい。












